Срочная публикация научной статьи
+7 995 770 98 40
+7 995 202 54 42
info@journalpro.ru
Эндоскопическое эндоназальное удаление оссифицирующих фибром полости носа и околоносовых пазух: серия случаев и обзор литературы
Рубрика: Медицинские науки
Журнал: «Евразийский Научный Журнал №4 2022» (апрель, 2022)
Количество просмотров статьи: 1556
Показать PDF версию Эндоскопическое эндоназальное удаление оссифицирующих фибром полости носа и околоносовых пазух: серия случаев и обзор литературы
Черникова Н.А.
ФГАУ «Национальный медицинский исследовательский
центр нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России,
4-я Тверская-Ямская ул., 16, Москва, Россия, 125047
E-mail: Chernikhope@gmail.com
Шелеско Е.В.
К.м.н.
ФГАУ «Национальный медицинский исследовательский
центр нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России,
4-я Тверская-Ямская ул., 16, Москва, Россия, 125047
E-mail: Eshelesko@nsi.ru
Снигирева Г.П.
к.б.н.
ФГАУ «Национальный медицинский исследовательский
центр нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России,
4-я Тверская-Ямская ул., 16, Москва, Россия, 125047
E-mail: sni_gal@mail.ru
Белов А.И.
к.м.н.
ФГАУ «Национальный медицинский исследовательский
центр нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России,
4-я Тверская-Ямская ул., 16, Москва, Россия, 125047
E-mail: aibelov@nsi.ru
Endoscopic endonasal removal of ossifying fibromas of the nose and paranasal sinuses: сase series and literature review.
Chernikova N.A., Federal State Autonomous Institution «N.N. Burdenko National Scientific and Practical Center for Neurosurgery» of the Ministry of Healthcare of the Russian Federation, 4-Tverskaya-Yamskaya Str. 16, Moscow, Russia, 125047 Chernikhope@gmail.com
Shelesko E.V., Federal State Autonomous Institution «N.N. Burdenko National Scientific and Practical Center for Neurosurgery» of the Ministry of Healthcare of the Russian Federation, 4-Tverskaya-Yamskaya Str. 16, Moscow, Russia, 125047, Eshelesko@nsi.ru
Snigireva G.P., Federal State Autonomous Institution «N.N. Burdenko National Scientific and Practical Center for Neurosurgery» of the Ministry of Healthcare of the Russian Federation, 4-Tverskaya-Yamskaya Str. 16, Moscow, Russia, 125047, sni_gal@mail.ru
Belov A.I. Federal State Autonomous Institution «N.N. Burdenko National Scientific and Practical Center for Neurosurgery» of the Ministry of Healthcare of the Russian Federation, 4-Tverskaya-Yamskaya Str. 16, Moscow, Russia, 125047, aibelov@nsi.ru
Аннотация
Оссифицирующая фиброма — это доброкачественная опухоль, которая развивается из периодонтальной связки.
Материалы и методы: В НМИЦН им. ак. Н. Н. Бурденко с 2009 по 2019 годы было прооперировано 61 пациент с костно-фиброзными образованиями полости носа и околоносовых пазух из них оссифицирующая фиброма встречалась в 10 (16,4%) случаях. Проведен ретроспективный анализ серии и обзор литературы в целях сравнения полученных данных с результатами других исследований.
Результаты: Чаще всего оссифицирующая фиброма локализовалась в решетчатом лабиринте — 8 (80%), опухоль распространялась в орбиту в половине случаев (5 — 50%). Клиновидная пазуха поражалась в 2 (20%) случаях, верхнечелюстная пазуха в 2 (20%) случаях, лобная пазуха была вовлечена в процесс в 1 (10%) случае. Все 10 пациентов проходили хирургическое лечение, эффективность которого составило 90%.
Выводы. Дифференциальную диагностику оссифицирующей фибромы необходимо проводить с фиброзной дисплазией, остеомой, аневризмальной костной кистой, десмопластической фибромой по клиническим, рентгенологическим и гистологическим данным. Лечение оссифицирующей фибромы хирургическое с использованием как наружных, так и эндоскопических доступов. Учитывая высокий риск рецидивов следует стремиться к радикальному удалению опухоли.
Abstract
Ossifying fibroma is a benign tumor that develops from the periodontal ligament.
Materials and Methods ak. N. N. Burdenko operated on 61 patients with bone-fibrous formations of the nasal cavity and paranasal sinuses from 2009 to 2019, of which ossifying fibroma occurred in 10 (16.4%) cases. A retrospective analysis of the series and a review of the literature were carried out in order to compare the obtained data with the results of other studies.
Results: Most often, ossifying fibroma was localized in the cribriform labyrinth — 8 (80%), the tumor spread into the orbit in half of the cases (5 — 50%). The sphenoid sinus was affected in 2 (20%) cases, the maxillary sinus in 2 (20%) cases, the frontal sinus was involved in the process in 1 (10%) case. All 10 patients underwent surgical treatment, the effectiveness of which was 90%.
Conclusions. Differential diagnosis of ossifying fibroma should be carried out with fibrous dysplasia, osteoma, aneurysmal bone cyst, desmoplastic fibroma according to clinical, radiological and histological data. Treatment of ossifying fibroma is surgical, using both external and endoscopic approaches. Given the high risk of recurrence, radical removal of the tumor should be sought.
Key words: Ossifying fibroma, cementoma, juvenile ossifying fibroma, bone fibrous lesions, endoscopic endonasal surgery.
Введение.
Оссифицирующая фиброма — это доброкачественная опухоль, которая развивается из периодонтальной связки [1]. Впервые эта опухоль была описана в 1927 году Montgomery [2]. До 1948 года данное заболевание рассматривали как вариант костно-фиброзной дисплазии [3]. Этиология этого заболевания до сих пор неизвестна, но важными факторами, описанными в литературе, могут быть генетические нарушения и травма [4,5]. По данным Всемирной Организации Здравоохранения при оссифицирующей фиброме происходит замещение нормальной кости фиброзной тканью, содержащей различное количество минерализованного материала и цемента. Такие поражения, в зависимости от соотношения цемента или кости, обозначаются как цементомы, оссифицирующие или цементно-оссифицирующие фибромы [6,7]. Заболевание встречается очень редко, поэтому в литературе нет точных статистических данных. Заболевание характерно для женщин 20-40 лет. Различают также ювенильную оссифицирующую фиброму, которая встречается у детей младше 16 лет и имеет склонность к агрессивному быстрому росту и рецидивированию [8].
Опухоль обладает медленным безболезненным ростом и на ранней стадии не сопровождается какой-либо симптоматикой. С увеличением размеров появляется односторонний отек, деформация лицевой области, смещение зубов, лицевые боли, нарушение носового дыхания, зрительные или глазодвигательные нарушения [9].
Диагностика оссифицирующих фибром полости носа и околоносовых пазух осуществляется на основании осмотра оториноларинголога, эндоскопического исследования полости носа компьютерной (КТ) и магнитно-резонансной (МРТ) томографии, верификации гистологического. Для лечения применяют хирургическую тактику [10].
В данной статье приводится наша серия случаев эндоскопического эндоназального лечения оссифицирующих фибром полости носа и околоносовых пазух.
Материалы и методы.
В НМИЦН им. ак. Н. Н. Бурденко с 2009 по 2019 годы было прооперировано 61 пациент с доброкачественными костно-фиброзными образованиями полости носа, околоносовых пазух и основания черепа. Оссифицирующая фиброма встречалась в 10 (16,4%) случаях. Проведен ретроспективный анализ серии: оценивался возраст, пол пациентов, клиническая картина, описания рентгенологических исследований (КТ, МРТ), интраоперационные данные. Всем пациентам проводилось хирургическое лечение с использованием эндоскопической стойки фирмы «Карл Шторц», Германия, включающую в себя монитор, HD- видеокамеру, галогеновый источник света. Также во время операций применяли комплект ригидных 4 мм эндоскопов с различными углами зрения — 0°, 30°, 45°, моно- и биполярную коагуляцию, дрель. Использовались стандартные эндоскопические инструменты и инструменты, изогнутые под различными углами, обеспечивающие возможность манипуляции в околоносовых пазухах.
Эффективность лечения оценивалась по анализу частоты рецидивов и осложнений в раннем (до 2 недель) и позднем послеоперационном периоде (в среднем до 4 лет). Проведен обзор литературы в целях сравнения полученных нами данных с результатами других исследований.
Результаты.
В серии из 10 человек — средний возраст составил 26 лет (диапазон — 4-66 лет) 7 (70%) — мужчины, 3 (30%) — женщины. В среднем появление жалоб отмечалось в период от 5 месяцев до 1 года. В основном пациентов беспокоили нарушение носового дыхания (6 случаев — 60%), заложенность носа (5 случаев — 50%). В 5 (50%) случаев у пациентов отмечался экзофтальм, так как образование распространялось в орбиту, а в 1 (10%) случае отмечены глазодвигательные нарушения в виде ограничения подвижности правого глазного яблока кнутри и кверху за счет компрессионного воздействия на экстраокулярные мышцы. Также было 2 (20%) случая возникновения онемения на лице за счет воздействия на ветви тройничного нерва. В большинстве случаев опухоль локализовалась справа (7 случаев — 70%). Чаще всего были вовлечены в процесс полость носа, клетки решетчатого лабиринта — 8 (80%), опухоль распространялась в орбиту в половине случаев (5 — 50%), клиновидная в 2 (20%) случаях, верхнечелюстная пазухи поражалась в 2 (20%) случаях, лобная пазуха была вовлечена в процесс в 1 (10%) случае.
Данные по возрасту, полу, локализации и клиническим проявлениям оссифицирующих фибром серии представлены в таблице 1.
Таблица 1. Данные по возрасту, полу, локализации и клиническим проявлениям оссифицирующих фибром в нашей серии.
| № | Возраст | Пол | Клиническая картина | Локализация |
| 1 | 57 | м | Нарушение носового дыхания, выделения из носа, онемение на лице, снижение слуха по кондуктивному типу | Полость носа, носоглотка, клиновидная пазуха справа |
| 2 | 8 | м | Нарушение носового дыхания, выделения из носа | Полость носа, клетки решетчатого лабиринта слева |
| 3 | 28 | м | Нарушение носового дыхания, выделения из носа | Полость носа, клетки решетчатого лабиринта справа |
| 4 | 16 | м | Нарушение носового дыхания, выделения из носа, экзофтальм, онемение на лице | Полость носа, клетки решетчатого лабиринта, орбита справа |
| 5 | 4 | м | Экзофтальм, глазодвигательные нарушения | Полость носа, клетки решетчатого лабиринта, орбита справа |
| 6 | 9 | ж | Нарушение носового дыхания | Клиновидная пазуха слева |
| 7 | 12 | ж | Нарушение носового дыхания, экзофтальм | Полость носа, лобная пазуха, клетки решетчатого лабиринта, орбита справа |
| 8 | 43 | м | Нарушение носового дыхания | Полость носа, клиновидная пазуха, клетки решетчатого лабиринта слева |
| 9 | 66 | ж | Экзофтальм | Полость носа, верхнечелюстная пазуха, клетки решетчатого лабиринта, орбита справа |
| 10 | 12 | м | Экзофтальм | Полость носа, верхнечелюстная пазуха, клетки решетчатого лабиринта, орбита справа |
Все 10 пациентов проходили хирургическое лечение. В 9 (90%) случаев выполняли эндоскопическое эндоназальное удаление образования. В 1 (10%) использовали комбинированный доступ: эндоскопический для удаления опухоли в полости носа и клетках решетчатого лабиринта, наружный трансфронтальный (через бикоронарный разрез) для удаления опухоли из лобной пазухи. Интраоперационная навигация использовалась в 4 (40%) случаях. В 3 случаях во время операции было отмечено распространение опухоли интракраниально. В одном случае во время операции отмечалась назальная ликворея в области ситовидной пластинки, в 2 случаях опухоль не прорастала в твердую мозговую оболочку, поэтому была удалена только поврежденная кость в области крыши решетчатого лабиринта в первом случае и задней стенки лобной пазухи во втором. Для пластики использовали тахокомб интракраниально и назосептальный лоскут на питающей ножке, уложенный поверх дефекта с его значительным перекрытием. Средний объем кровопотери во время операций составил 260 мл (диапазон от 50 до 1000 мл).
По данным морфологического исследования в биоптатах выявлялись фрагменты ткани опухоли, сформированной полями мономорфных веретеновидных клеток, при этом ядра клеток были вытянутой и овальной формы со слабо выраженным полиморфизмом, содержали глыбчатый хроматин. В строме опухоли определялись редкие петрификаты, представленные минерализованной костной тканью. По периферии образований прослеживалась реактивная оссификация, представленная незрелой костной тканью волокнистого строения по типу «woven bone». Митотическая активность и очаги некроза не были обнаружены. По данным иммуногистохимического исследования с антителами к vimentin, CK19, SMA, p53, CD34, Ki-67, PanCK, EMA, desmin, S-100, beta-catenin, MDM2, cdk4 в ткани опухоли выявлена экспрессия виментина фокальная экспрессия SMA, локус экспрессии beta-catenin — цитоплазматический, в эндотелии сосудов определяется экспрессия CD34. Пролиферативная активность ИМ Ki-67 около 8%. Реакции с остальными антителами (CK19, p53, CD68, PanCK, S-100, MDM2, cdk4, EMA, десмин) в ткани опухоли в пределах исследованого материала не обнаружены (рисунок 1 а, б).

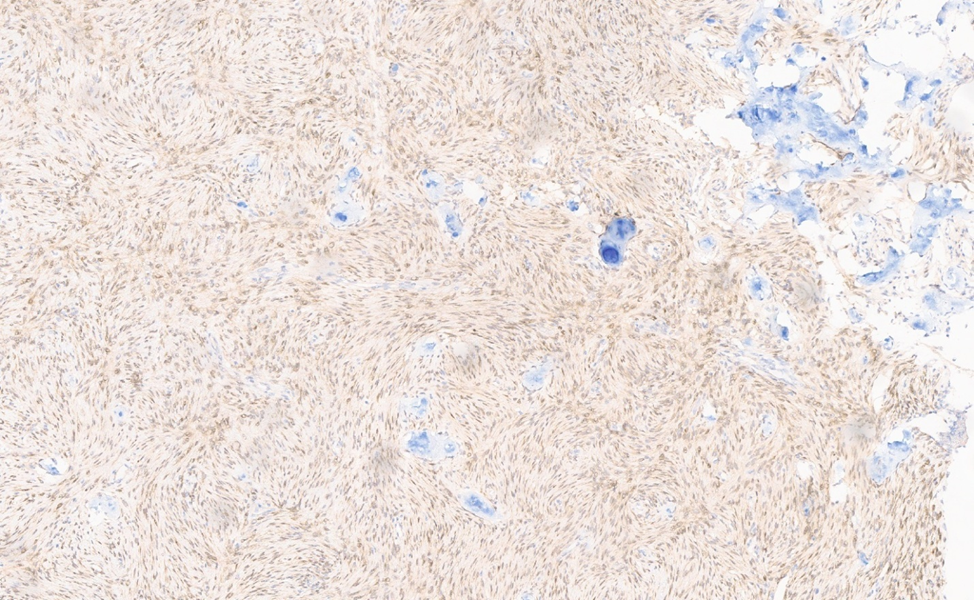
Рисунок 1 а,б Микрофотографии, демонстрирующие особенности, характерные для оссифицирующей фибромы 1а фрагменты ткани опухоли, сформированной полями мономорфных веретеновидных клеток, ядра клеток были вытянутой и овальной формы. В строме опухоли редкие петрификаты, по периферии реактивная оссификация (Гемотоксилин и эозин, х200).
1 б Иммуногистохимический препарат с экспрессией CD34.
Figure 1 a, b Micrographs showing the features characteristic of ossifying fibroma. 1a, fragments of tumor tissue formed by fields of monomorphic spindle cells, cell nuclei were elongated and ovals. There are rare petrification in the tumor stroma, reactive ossification along the periphery (Hemotoxylin and eosin, x200).
1 b Immunohistochemical preparation with expression of CD34.
У пациентов не было отмечено осложнений в раннем и позднем послеоперационном периоде. У одного пациента (10%) отмечался рецидив через 4 года после операции. Симптоматика и распространенность опухоли была, как и при первой операции. Пациенту выполнена эндоскопическое эндонозальное удаление образования. В дальнейшем не было отмечено рецидивов спустя 2 года после повторной операции.
Дискуссия.
Оссифицирующие фибромы относятся к доброкачественным фиброзно-костным поражениям [11]. Патогенез мало изучен, в связи с редкостью заболевания. В 1995 году Sawyer и его коллеги [12] сообщили о наличии хромосомных мутациях — Xq26 и 2q33 у пациентов с оссифицирующими фибромами. Авторами описано два клинических случая, в которых наблюдалась транслокация (X; 2) (q26; q33) как единственная аномалия. По их данным в результате мутации происходит рост опухоли из мезенхимы периодонтальной связки, клетки которой производят цементную, костную или волокнистую ткань.
Также в литературе встречаются предположения, что на рост опухоли влияет травматический фактор. Так Wenig BL и соавторы [13] описали случай развития оссифицирующей фибромы у пациента после краниофациальной травмы. В дальнейшем стали появляться другие случаи, подтверждающие влияние травматического фактора на патогенез роста опухоли. В нашей серии у пациентов не было отмечено травм в анамнезе.
В настоящее время классификация оссифицирующей фибромы несколько трудна, так как используются множество иногда перекрывающих друг друга терминов (оссифицирующая фиброма, цементирующая фиброма, цементо-оссифицирующая фиброма, псаммо-остеоидная фиброма, псаммоматоидная оссифицирующая фиброма, ювенильная оссифицирующая фиброма, ювенильная агрессивная оссифицирующая фиброма) [14].
С клинической точки зрения представляется обоснованным разделение этого заболевания на ювенильную оссифицирующую фиброму и цементо-оссифицирующую фиброму, что связано с различным течением и прогнозом лечения опухоли в этих группах.
Ювенильная оссифицирующая фиброма возникает у детей до 16 лет и обладает более агрессивным и быстрым ростом. Она характеризуется высокой частотой рецидивов после хирургического удаления [15]. В нашей серии встречалось 4 (40%) случая оссифицирующей фибромы у детей до 16 лет. Был рецидив у одного ребенка спустя 4 года операции. Ребенку выполнили повторное эндоскопическое удаление опухоли. При динамическом наблюдении в течение 2 лет не было отмечено роста образования. Также в серии был ребенок, которому первично удаляли опухоль по месту жительства, и он поступил в НМИЦН им. ак. Н.Н. Бурденко для повторной операции. После удаления оссифицирующей фибромы пациента наблюдали в течение 3 лет. В течение этого периода не было отмечено рецидива опухоли.
Цументо-оссифицирующая фиброма возникает в более взрослом возрасте в возрасте от 20 до 40 лет и обладает менее худшим прогнозом, так как редко рецидивируют после полной резекции опухоли [16]. В нашей серии не было отмечено рецидивов у пациентов старше 20 лет.
Su и соавторы [17] сообщают, что в 70% случаев оссифицирующая фиброма поражает нижнюю челюсть, в 22% — верхнюю челюсть, поражение клеток решетчатого лабиринта, клиновидной, лобной пазухи является единичными случаями. В нашей серии наиболее частой локализацией оказался решетчатый лабиринт с распространением в орбиту — 8 (80%) случаев.
Место исходного роста оссифицирующей фибромы, при локализации удаленной от периодонтальной связки (орбита, лобная пазуха, клиновидная пазуха) не полностью изучено. Возможно, опухоль происходит из атипично расположенных клеток периодонтальной связки вследствие нарушения эмбриогенеза или из других клеток, способных производить цемент, кость и волокнистую ткань [18]. Интересным является тот факт, что в области орбиты оссифицирующие фибромы содержат мало цемента. Опухоль имеет овальные или круглые кальцифицированные конкременты с концентрическими расслоениями (псаммоматоидные тельца) и, как правило, обладает агрессивным ростом с распространением в соседние анатомические области с разрушением костных структур [19].
На начальных стадиях пациенты не отмечают никаких симптомов. Наиболее распространенными клиническими симптомами являются нарушение носового дыхания, риногенная гипосмия или аносмия, выделения из носа. Другие симптомы связаны с распространением образования на соседние органы и ткани, включают в себя экзофтальм, эпифору (слезотечение), головные боли, анестезию в лицевой области. Опухоль обладает медленном ростом [20,21]. В нашей серии период между появлением первых симптомов и обращением в стационар составило в среднем 12 месяцев (диапазон 1 — 30 месяцев).
Для диагностики использовались КТ и МРТ, которые показывали структуру опухоли, локализацию и отношение к соседним органам.
Особенности рентгенологических данных зависят от стадии развития опухоли, а также от количества минерализованной матрицы. Начальным проявлением опухоли на рентгенограмме является образование участка разряжения костной ткани правильной формы с четкими контурами. По мере роста опухоли зона разряжения увеличивается, могут встречаться кисты. На МРТ-изображениях в T1-взвешенном режиме оссифицирующие фибромы выглядят неоднородно и обычно показывают промежуточный сигнал, в Т2-взвешенном режиме для них характерен гипоинтенсивный сигнал. При выполнении МРТ с контрастом (гадолиний) отмечается умеренное накопление контраста в T1-взвешенном режиме [22,23].
Дифференциальный диагноз прежде всего проводят с костно-фиброзными образованиями и опухолями кости: остеомами, фиброзной дисплазией, десмопластической фибромой, аневризмальной костной кистой, остеосаркомой [24].
Компьютерная томография с контрастом может показать усиление сигнала, соответствующее мягким тканям оссифицирующей фибромы, в то время как сигнал от остеом не усиливаются. Резко очерченные внешние границы оссифицирующей фибромы являются наиболее важным рентгенологическим признаком для дифференциальной диагностики с фиброзной дисплазией и злокачественными опухолями, такими как саркома или хондросаркома, которые обладают инвазивными ростом [25] (рисунок 2).

Рисунок 2. КТ околоносвых пазух фронтальная проекция. Оссифицирующая фиброма полости носа, клеток решетчатого лабиринта, верхнечелюстной пазухи с распространением в орбиту справа.
Figure 2. CT of the paranasal sinuses, frontal view. Ossifying fibroma of the nasal cavity, ethmoid labyrinth cells, maxillary sinus spreading into the orbit on the right.
На поздних стадиях оссифицирущая фиброма может образовывать кисты, что необходимо помнить при дифференциальной диагностике с аневризмальной костной кистой [26]. В таких случаях стоит опираться не только на рентгенологические, но и на клинические данные (таблица 2)
Таблица 2. Дифференциальная диагностика оссифицирующих фибром

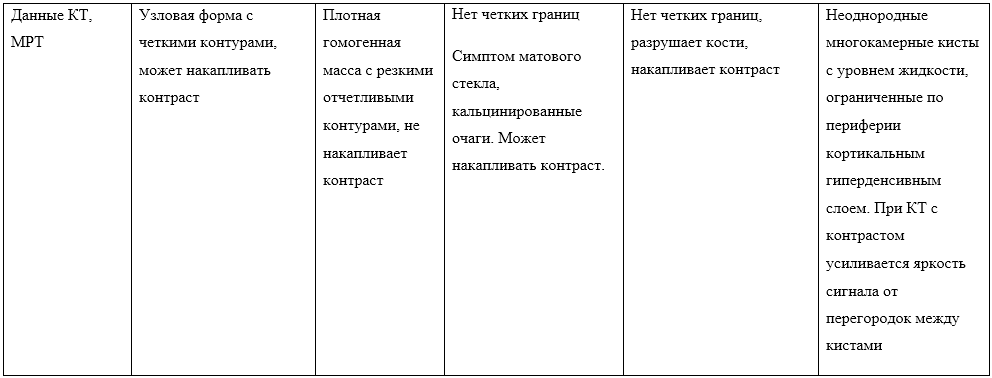
ЧМН — черепно-мозговые нервы
Однако для постановки точного диагноза требуется гистологическое исследование. Микроскопически оссифицирующие фибромы построены из фиброзной стромы с включением разного количества незрелой кости (перепончатой ретикулофиброзной, не обладающей упорядоченной структурой) и более зрелой пластинчатой кости. Нормально сформированный костный мозг и сосудистая система отсутствует. Фиброма отграничена от здоровой костной ткани четким кортикальным ободком, в просвете образования формируются единичные мелкие кальцификаты и/или плотные включения, имеющие строение цементиклей [27].
Костный компонент обычно неоднородный: центральные части часто фиброзные, а периферические отделы содержат пластинчатую кость. Полное созревание кости наблюдается редко. Фиброзная строма может быть плотно клеточной; митотические фигуры редко отсутствуют. Могут наблюдаться вторичные изменения, включая кровоизлияния, кисты, воспаление и гигантские клетки. Существуют два гистологических варианта оссифицирующей фибромы: трабекулярный и псаммоматоидный [28]. Трабекулярный вариант оссифицирующей фибромы необходимо прежде всего дифференцировать с фиброзной дисплазией. Основным различительным признаком является отсутствие при фиброзной дисплазии демаркационной разграничительной зоны от здоровой прилежащей кости. Данный признак, как правило, определяется хирургом во время оперативного вмешательства. Псаммоматоидный вариант необходимо дифференцировать с псаммоматоидной менингиомой. Некоторые гистологические признаки, как, например, отсутствие гигантских клеток, остеобластического римминга трабекул, а также хаотичное расположение псаммомных телец, помогают в дифференциальной диагностике [29]. Псаммоматоидная менингиома, как правило, проявляет иммунореактивность к ЕМА и S-100 Protein, в то время как оссифицирующая фиброма не экспрессирует данных маркеров, чаще позитивна к SMA и CD10 [30].
Тактика лечения оссифицирующих фибром — хирургическая. Лучевая терапия противопоказана из-за повышенного риска злокачественной трансформации, которая может возникнуть с частотой от 0,4 до 40% [31]. Ledderose и соавторы [32] в своей статье сообщают, что возможна выжидательная тактика при бессимптомных оссифицирующих фибромах у взрослых. По их данным в двух случаях не было прогрессирования опухоли в течение 2 лет после выполнения эндоскопической биопсии и установки диагноза. Однако этих данных недостаточно и требуются исследования на большем количестве пациентов и наблюдений в течение длительного времени.
Хирургическое лечение заключается в энуклиации опухолевого узла. Для предупреждения рецидива опухоль необходимо удалять полностью. В литературе указывается, что частота рецидивов варьирует от 5 до 30% у взрослых, а при ювенильной оссифицирующей фиброме 30-58%. Рецидивы, вероятно, связаны с неполным удалением опухоли при широком распространении [33,34].
В литературе описаны доступы и методики удаления этих новообразований. Раньше использовались экстраназальный и микроскопические методы. Troulis и коллеги [35] описывают методику удаления опухоли наружным доступом с последующей реконструкцией челюсти в 4 этапа.
С развитием техники стали применяться малоинвазивные эндоскопические методы. Cinglio Appiani и соавт. [36] в своей статье описывают 11 случаев оссифицирующих фибром. Для лечения они применяли эндоскопический эндоназальный доступ в большинстве случаев. Наружный доступ использовался при расположении оссифицирующей фибромы в лобной пазухе и в случае распространения опухоли за пределы верхнечелюстной пазухи кпереди. Авторы сообщают, что несмотря на то, что опухоль богато васкуляризирована, предоперационная эмболизация противопоказана, так как кровоснабжение чаще всего осуществляется за счет глазной артерии. При этом возможна окклюзия центральной артерии сетчатки и полная слепота.
В нашей серии в основном (90%) применялось эндоскопическое эндоназальное удаление опухоли. Рецидив возник у одного пациента спустя 4 года после операции. В дальнейшем была выполнена повторная операция. Сравнение наших данных с данными мировой литературы представлены в таблице 3.
Таблица 3. Данные мировой литературы лечения оссифицирующих фибром полости носа и коолоносовых пазух
| Автор, год | Кол-во наблюдений | Средний возраст | Хирургический доступ | Эффективность лечения |
| Slootweg, 1993 [37] | 3 | 25 | Наружный | 100% |
| Wenig, 1995 [38] | 7 | 33 | 6 Наружный 1 Эндоскопический | 85,7% |
| Lawton, 1997 [39] | 4 | 28 | 3 Наружный 1 Эндоскопический | 100% |
| Harstein, 1998 [40] | 3 | 16 | Наружный доступ | 100% |
| Ledderose, 2011 [32] | 5 | 49 | Эндоскопический | 100% |
| Wang, 2014 [41] | 31 | 25 | 26 Эндоскопический 5 Наружный | 87% |
| Jack J. Liu, 2017 [33] | 13 | 37 | 10 Наружный 3 Эндоскопический | 77% |
| НМИЦН им. Н. Н. Бурденко | 10 | 20 | 9 Эндоскопический 1 Наружный | 90% |
Как видно из таблицы самая большая серия была описана Wang и соавторами [41] в 2014 году. Авторы описывают в своей статье серию из 31 случая ювенильных оссифицирующих фибром. В связи с агрессивным быстрым ростом опухоли в детском возрасте, высокой васкуляризации и выработкой основного фактора роста фибробластов авторы рекомендуют проводить удаление опухоли в сочетании с адьювантной терапией альфа-интерферонами в течение года. После хирургического лечения рекомендуют длительное наблюдение и контроль. Liu и соавторы [33] проводили многоцентровое исследование. По их данным эндоскопическое эндоназальное удаление оссифицирующих фибром является эффективным и безопасным методом. Наружные доступы показаны при запущенном процессе, когда невозможно удалить образование эндоскопическим доступом полностью.
Выводы.
1. Оссифицирующая фиброма — это редкая доброкачественная опухоль, склонная к агрессивному росту, особенно в детском возрасте.
2.Дифференциальную диагностику оссифицирующей фибромы необходимо проводить с фиброзной дисплазией, остеомой, аневризмальной костной кистой, десмопластической фибромой по клиническим, рентгенологическим и гистологическим данным.
3. Лечение оссифицирующей фибромы хирургическое с использованием как наружных, так и эндоскопических доступов. Учитывая высокий риск рецидивов следует стремиться к радикальному удалению опухоли.
Сведения об авторах
Врач Надежда Алексеевна Черникова. N.A. Chernikova, https://orcid.org/0000-0002-4895-233X. Chernikhope@gmail.com, тел 89654208719 — связь с редакцией.
к.м.н. Елизавета Владимировна Шелеско E.V. Shelesko https://orcid.org/0000-0002-8249-9153, Eshelesko@nsi.ru , тел.+7 926 923-29-91
Доктор биологических наук Снигирева Галина Петровна, G.P. Snigireva https://orcid.org/0000-0003-2654-8210, sni_gal@mail.ru, тел. +7 (910) 422-41-90
Ординатор Никонова Светлана Дмитриевна, S.D. Nikonova,
Кандидат медицинских наук Александр Иванович Белов, A.I. Belov, https://orcid.org/0000-0003-0269-2138 aibelov@nsi.ru, тел: 7 916 657-67-69
Литература/ References
1. Khan SA, Sharma NK, Raj V, Sethi T. Ossifying fibroma of maxilla in a male child: Report of a case and review of literature. Natl J Maxillofac Surg 2011; 2:73–79. https://doi.org/10.4103/0975-5950.85859
2. Montgomery AH. Ossifying fibroma of the jaw. Arch Surg 1927;15:30 — 44. https://doi.org/10.1001/archsurg.1927.01130190033002
3. J M Walter Jr, B C Terry, E W Small, S R Matteson, R M Howell Aggressive ossifying fibroma of the maxilla: review of the literature and report of case. J Oral Surg 1979; 37: 276 — 86
4. El-Mofty S. Psammomatoid and trabecular juvenile ossifying fibroma of the craniofacial skeleton: two distinct clinicopathologic entities. Oral. Surg. Oral. Med. Oral. Pathol. Oral. Radiol. Endod. 2002; 93:296-304 https://doi.org/10.1067/moe.2002.121545
5. Yilmaz I, Bal N, Ozluoglu LN Isolated cementoossifying fibroma of the ethmoid bulla: a case report. Ear Nose Throat J 2006; 85:322–324 https://doi.org/10.1177/014556130608500512
6. Rashi Bahl, Sumeet Sandhu, Mohita Gupta. Benign fibro-osseus lesions of jaws — a review. International Dental Journal of Student’s Research. 2012, 1 (2):56-68.
7. Goetz Brademann, Jochen A. Werner, Ute Jänig, Hubertus M. Mehdorn, Heinrich Rudert Cemento-ossifying fibroma of the petromastoid region: case report and review of the literature. J Laryngol Otol 1997;111:152-5. https://doi.org/10.1017/s0022215100136709
8. Marvel JB, Marsh MA, Catlin FI Ossifying fibroma of the mid-face and paranasal sinuses: diagnostic and therapeutic considerations. Otolaryngol Head Neck Surg 1991; 104:803–808 https://doi.org/10.1177/019459989110400606
9. Maria E. Papadaki, Maria J. Troulis, Leonard B. Kaban Advances in Diagnosis and Management of Fibro-Osseous Lesions Oral Maxillofacial Surg Clin N Am 2005; 17:415 — 434 https://doi.org/10.1016/j.coms.2005.06.004
10. Roy Eversole, Lan Su, Samir ElMoftu. Benign fibro-osseus lesions of the craniofacial complex. A review. Head and Neck Pathol 2008; 2:177-202 https://doi.org/10.1007/s12105-008-0057-2
11. Smith SF, Newman L, Walker DM, Papadopoulos H. Juvenile aggressive psammomatoid ossifying fibroma: an interesting, challenging, and unusual case report and review of the literature. Journal of Oral and Maxillofacial Surgery 2009;67(1):200—6 https://doi.org/10.1016/j.joms.2007.12.009
12. Jeffrey R. Sawyer, A. Frandne Tryka, Jane M. Bell, Frederick A. Boop Nonrandom chromosome breakpoints at Xq26 and 2q33 characterize cemento-ossifying fibromas of the orbit. Cancer 1995;76(10):1853 — 9 https://doi.org/10.1002/1097-0142(19951115)76:10<1853::aid-cncr2820761026>3.0.co;2-d
13. B L Wenig, J J Sciubba, A Cohen, M N Goldstein, A L Abramson A destructive maxillary cemento-ossifying fibroma following maxillofacial trauma Laryngoscope 1984;94(6):810-5. https://doi.org/10.1288/00005537-198406000-00015.
14. Post G, Kountakis SE Endoscopic resection of large sinonasal ossifying fibroma. Am J Otolaryngol 2005; 26:54–56 https://doi.org/10.1016/j.amjoto.2004.06.009
15. Cotua Quintero C, Saab Mazzei A, Revuelta Barbero J, Parajon Diaz A, Ley Urzaiz L. Juvenile psammomatoid ossifying fibroma of the posterior fossa: a case report and review. Springerplus 2016;5:1089 https://doi.org/10.1186/s40064-016-2758-4
16. London SD, Schlosser RJ, Gross CW Endoscopic management of benign sinonasal tumors: a decade of experience. Am J Rhinol 2002; 16:221–227 https://doi.org/10.1177/194589240201600408
17. Su L, Weathers DR, and Waldron CA. Distinguishing features of focal cemento-osseous dysplasia and cemento-ossifying fibromas. A clinical and radiologic spectrum of 316 cases. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 1997; 84:540 —549 https://doi.org/10.1016/s1079-2104(97)90271-7
18. B M Wenig , MF Mafee, L Ghosh Fibro-osseous, osseous, and cartilaginous lesions of the orbit and paraorbital region. Correlative clinicopathologic and radiographic features, including the diagnostic role of CT and MR imaging Radiol Clin North Am 1998;36(6):1241-59, https://doi.org/10.1016/s0033-8389(05)70243-8
19. N H Ta , A Addison, B Beigi, C Philpott Unilateral visual loss resulting from orbital encroachment of an ethmoidal juvenile trabecular ossifying fibroma Ann R Coll Surg Engl 2019;101(4):e111-e114. https://doi.org/10.1308/rcsann.2019.0030
20. R Peter Manes, Matthew W Ryan, Pete S Batra, Dianne Mendelsohn, Yisheng V Fang, Bradley F Marple Ossifying fibroma of the nose and paranasal sinuses. int Forum Allergy rhinol 2013;3:161-8 https://doi.org/10.1002/alr.21067.
21. Al-Mazrou KA, Mansoor A, Payne M, Richardson MA. Ossifying fibromyxoid tumor of the ethmoid sinus in a newborn: report of a case and literature review. int J Pediatr otorhinolaryngol 2004;68:225-30. https://doi.org/10.1016/j.ijporl.2003.09.016.
22. V. Engelbrecht, S. Preis, W. Hassler, H. G. Lenard CT and MRI of congenital sinonasal ossifying fibroma. Neuroradiology 1999;41:526-9 https://doi.org/10.1007/s002340050798
23. Kendi AT, Kara S, Altinok D, Keskil S. Sinonasal ossifying fibroma with fluid fluid levels on MR images. AJnr Am J neuroradiol 2003;24:1639-41.
24. Aldo Suarez-Soto 1, Mari-Carmen Baquero-Ruiz de la Hermosa, Ignacio Minguez-Martínez, Luis-Miguel Floría-García, Jose Barea-Gámiz, Jose Delhom-Valero, Presentation Risueño-Mata Management of fibro-osseous lesions of the craniofacial area. Presentation of 19 cases and review of the literature Med Oral Patol Oral Cir Bucal 2013; 1;18(3):e479-85. https://doi.org/10.4317/medoral.18289.
25. Guy Efune, Carlos L Perez, Liyue Tong, Jordan Rihani, Pete S Batra Paranasal sinus and skull base fibro-osseous lesions: when is biopsy indicated for diagnosis? Int Forum Allergy Rhinol 2012;2(2):160-5. https://doi.org/10.1002/alr.20109.
26. B.T. Yang, Y.Z. Wang, X.Y. Wang, Z.C. Wang Imaging study of ossifying fibroma with associated aneurysmal bone cyst in the paranasal sinus. eur J radiol 2012;81:3450-5. https://doi.org/10.1016/j.ejrad.2012.05.010
27. Д.В. Рогожин, Ф. Бертони, Д. Ванэль, М. Гамбаротти, А. Риги, И.В. Булычева, Д.М. Коновалов, А. Г. Талалаев, В.Ю. Рощин, М.В. Болотин, А.В. Лопатин Доброкачественные фиброзно-костные поражения краниофациальной зоны у детей и подростков: анализ 28 случаев Cаркомы костей, мягких тканей и опухоли кожи 2014; 3—4— 65-73 (In Russ.). https://doi.org/10.17116/patol201577463-70
28. Д.В. Рогожин, И.В. Булычева Ювенильная оссифицирующая фиброма у детей. Особенности дифференциальной диагностики Cаркомы костей, мягких тканей и опухоли кожи № 1–2014: 70-73 (In Russ.).
29. Slootweg P.J., Panders A.K., Koopmans R., Nikkels P.G. Juvenile ossifying fibroma. An analysis of 33 cases with emphasis on histopathological aspects. J. Oral. Pathol. Med.1998; 23:385-388 https://doi.org/10.1111/j.1600-0714.1994.tb00081.x
30. Slootweg P.J. Maxillofacial fibro-osseous lesions: classification and differential diagnosis. Semin. Diagn. Pathol. 1996; 13:103-112.
31. Baumann I, Zimmermann R, Dammann F, Maassen MM. Ossifying fibroma of the ethmoid involving the orbit and the skull base. Otolaryngol Head Neck Surg 2005;133:158—159 https://doi.org/10.1016/j.otohns.2004.09.121
32. Georg J Ledderose 1, Klaus Stelter, Sven Becker, Andreas Leunig Paranasal ossifying fibroma: endoscopic resection or wait and scan? Eur Arch Otorhinolaryngol 2011 268(7):999-1004. https://doi.org/10.1007/s00405-011-1503-4.
33. Jack J Liu, Lester D R Thompson, Agnieszka M Janisiewicz, Terry Y Shibuya, David B Keschner, Rohit Garg, Jivianne T Lee Ossifying fibroma of the maxilla and sinonasal tract: Case series Allergy Rhinol (Providence) 2017 1;8(1):32-36. https://doi.org/10.2500/ar.2017.8.0190.
34. Abuzinada S, and Alyamani A. Management of juvenile ossifying fibroma in the maxilla and mandible. J Maxillfac Oral Surg 2010;9:91—95. https://doi.org/10.1007/s12663-010-0027-6
35. Maria J Troulis 1, W Bradford Williams, Leonard B Kaban Staged protocol for resection, skeletal reconstruction, and oral rehabilitation of children with jaw tumors J Oral Maxillofac Surg 2004 ;62(3):335-43. https://doi.org /10.1016/j.joms.2003.07.006.
36. M Ciniglio Appiani, B Verillaud, D Bresson, E Sauvaget, J-P Blancal, J-P Guichard, J-P Saint Maurice, M Wassef , A Karligkiotis, R Kania , P Herman Ossifying fibromas of the paranasal sinuses: diagnosis and management Acta Otorhinolaryngol Ital 2015;35(5):355-61. https://doi.org/10.14639/0392-100X-533.
37. Slootweg PJ, Panders AK, Nikkels PG. Psammomatoid ossifying fibroma of the paranasal sinuses. An extragnathic variant of cemento-ossifying fibroma. Report of three cases. J Craniomaxillofac Surg. 1993 21(7):294-7. https://doi.org/10.1016/s1010-5182(05)80350-6.
38. Wenig BM, Vinh TN, Smirniotopoulos JG, Fowler CB, Houston GD, Heffner DK. Aggressive psammomatoid ossifying fibromas of the sinonasal region: a clinicopathologic study of a distinct group of fibro-osseous lesions. Cancer. 1995 1;76(7):1155-65. https://doi.org/10.1002/1097-0142(19951001)76:7<1155::aid-cncr2820760710>3.0.co;2-p.
39. M T Lawton 1, J E Heiserman, S W Coons, B D Ragsdale, R F Spetzler Juvenile active ossifying fibroma. Report of four cases J Neurosurg 1997;86(2):279-85. https://doi.org/10.3171/jns.1997.86.2.0279.
40. M E Hartstein 1, A S Grove Jr, J J Woog, J W Shore, M P Joseph The multidisciplinary management of psammomatoid ossifying fibroma of the orbit Ophthalmology 1998 Apr;105(4):591-5. https://doi.org/10.1016/S0161-6420(98)94009-X.
41. Wang H, Sun X, Liu Q, Wang J, Wang D. Endoscopic resection of sinonasal ossifying fibroma: 31 cases report at an institution. Eur Arch Otorhinolaryngol. 2014;271(11):2975-82. https://doi.org/10.1007/s00405-014-2972-z.









