–°—А–Њ—З–љ–∞—П –њ—Г–±–ї–Є–Ї–∞—Ж–Є—П –љ–∞—Г—З–љ–Њ–є —Б—В–∞—В—М–Є
+7 995 770 98 40
+7 995 202 54 42
info@journalpro.ru
–Э–∞—А—Г—И–µ–љ–Є—П–Љ–Є —Б–µ—А–і–µ—З–љ–Њ–≥–Њ —А–Є—В–Љ–∞ –Є –∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –∞—А—Е–Є—В–µ–Ї—В–Њ–љ–Є–Ї–Є —Б–µ—А–і—Ж–∞ –њ—А–Є –≥–Є–њ–µ—А—В—А–Њ—Д–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А–і–Є–Њ–Љ–Є–Њ–њ–∞—В–Є–Є
–†—Г–±—А–Є–Ї–∞: –Ь–µ–і–Є—Ж–Є–љ—Б–Ї–Є–µ –љ–∞—Г–Ї–Є
–Ц—Г—А–љ–∞–ї: «–Х–≤—А–∞–Ј–Є–є—Б–Ї–Є–є –Э–∞—Г—З–љ—Л–є –Ц—Г—А–љ–∞–ї вДЦ4 2018» (–∞–њ—А–µ–ї—М, 2018)
–Ъ–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ—А–Њ—Б–Љ–Њ—В—А–Њ–≤ —Б—В–∞—В—М–Є: 2433
–Я–Њ–Ї–∞–Ј–∞—В—М PDF –≤–µ—А—Б–Є—О –Э–∞—А—Г—И–µ–љ–Є—П–Љ–Є —Б–µ—А–і–µ—З–љ–Њ–≥–Њ —А–Є—В–Љ–∞ –Є –∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –∞—А—Е–Є—В–µ–Ї—В–Њ–љ–Є–Ї–Є —Б–µ—А–і—Ж–∞ –њ—А–Є –≥–Є–њ–µ—А—В—А–Њ—Д–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А–і–Є–Њ–Љ–Є–Њ–њ–∞—В–Є–Є
–°–Ї–∞–Ї—Г–љ –Я–∞–≤–µ–ї –Т–∞–і–Є–Љ–Њ–≤–Є—З
Skakun Pavel Vadimovich
–°—В—Г–і–µ–љ—В
–С–µ–ї–Њ—А—Г—Б—Б–Ї–Є–є –≥–Њ—Б—Г–і–∞—А—Б—В–≤–µ–љ–љ—Л–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–є —Г–љ–Є–≤–µ—А—Б–Є—В–µ—В
–†–µ—Б–њ—Г–±–ї–Є–Ї–∞ –С–µ–ї–∞—А—Г—Б—М
–У—Г–±–Є—З–µ–≤–∞ –Р–ї–µ–Ї—Б–∞–љ–і—А–∞ –Т–∞—Б–Є–ї—М–µ–≤–љ–∞
Gubicheva Alexandra Vasilievna
–°—В—Г–і–µ–љ—В
–С–µ–ї–Њ—А—Г—Б—Б–Ї–Є–є –≥–Њ—Б—Г–і–∞—А—Б—В–≤–µ–љ–љ—Л–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–є —Г–љ–Є–≤–µ—А—Б–Є—В–µ—В
–†–µ—Б–њ—Г–±–ї–Є–Ї–∞ –С–µ–ї–∞—А—Г—Б—М
–Р–љ–љ–Њ—В–∞—Ж–Є—П. –У–Є–њ–µ—А—В—А–Њ—Д–Є—З–µ—Б–Ї–∞—П –Ї–∞—А–і–Є–Њ–Љ–Є–Њ–њ–∞—В–Є—П —З–∞—Б—В–Њ —Б–Њ—З–µ—В–∞–µ—В—Б—П —Б —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –љ–µ–і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–є –і–Є—Б–њ–ї–∞–Ј–Є–Є —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є, –Њ–і–љ–Є–Љ –Є–Ј –њ—А–Њ—П–≤–ї–µ–љ–Є–є –Ї–Њ—В–Њ—А–Њ–≥–Њ —П–≤–ї—П–µ—В—Б—П —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –Љ–∞–ї—Л—Е –∞–љ–Њ–Љ–∞–ї–Є–є —Б–µ—А–і—Ж–∞ (–Ь–Р–°), —П–≤–ї—П—О—Й–Є—Е—Б—П —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –љ–∞—А—Г—И–µ–љ–Є–є —А–Є—В–Љ–∞, —З—В–Њ –≤–∞–ґ–љ–Њ –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –У–Ъ–Ь–Я.
Abstract. Hypertrophic cardiomyopathy is often combined with the syndrome of undifferentiated connective tissue dysplasia, one of the manifestations of which is the formation of small heart anomalies (MAS), which are risk factors for the development of rhythm disturbances, which are important in the diagnosis of HCM.
–Ъ–ї—О—З–µ–≤—Л–µ —Б–ї–Њ–≤–∞: –≥–Є–њ–µ—А—В—А–Њ—Д–Є—З–µ—Б–Ї–∞—П –Ї–∞—А–і–Є–Њ–Љ–Є–Њ–њ–∞—В–Є—П, –Љ–∞–ї—Л–µ –∞–љ–Њ–Љ–∞–ї–Є–Є —Б–µ—А–і—Ж–∞, –љ–∞—А—Г—И–µ–љ–Є—П —А–Є—В–Љ–∞.
Key words: hypertrophic cardiomyopathy, small heart anomalies, rhythm disturbances.
–У–Є–њ–µ—А—В—А–Њ—Д–Є—З–µ—Б–Ї–∞—П –Ї–∞—А–і–Є–Њ–Љ–Є–Њ–њ–∞—В–Є—П (–У–Ъ–Ь–Я) –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –∞—Г—В–Њ—Б–Њ–Љ–љ–Њ-–і–Њ–Љ–Є–љ–∞–љ—В–љ—Л–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ —Б –љ–µ–њ–Њ–ї–љ–Њ–є –њ–µ–љ–µ—В—А–∞–љ—В–љ–Њ—Б—В—М—О, —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–µ–µ—Б—П —Г—В–Њ–ї—Й–µ–љ–Є–µ–Љ —Б—В–µ–љ–Ї–Є –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ (–Ы–Ц) –Є/–Є–ї–Є –≤ —А–µ–і–Ї–Є—Е —Б–ї—Г—З–∞—П—Е вАФ –њ—А–∞–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞, —З–∞—Й–µ –∞—Б–Є–Љ–Љ–µ—В—А–Є—З–љ–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞, –Ј–∞ —Б—З–µ—В —Г—В–Њ–ї—Й–µ–љ–Є—П –Љ–µ–ґ–ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤–Њ–є –њ–µ—А–µ–≥–Њ—А–Њ–і–Ї–Є, —А–∞–Ј–≤–Є–≤–∞—О—Й–µ–≥–Њ—Б—П –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Љ—Г—В–∞—Ж–Є–Є —Б–Њ–Ї—А–∞—В–Є—В–µ–ї—М–љ—Л—Е –±–µ–ї–Ї–Њ–≤ –Љ–Є–Њ–Ї–∞—А–і–∞
–Я–Њ –і–∞–љ–љ—Л–Љ –њ–Њ—Б–ї–µ–і–љ–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ—А–Є –У–Ъ–Ь–Я —З–∞—Б—В–Њ –љ–∞–±–ї—О–і–∞—О—В—Б—П –њ—А–Є–Ј–љ–∞–Ї–Є —Б–Є–љ–і—А–Њ–Љ–∞ –љ–µ–і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–є –і–Є—Б–њ–ї–∞–Ј–Є–Є —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є, —З–∞—Б—В—Л–Љ–Є –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ–Є –Ї–Њ—В–Њ—А–Њ–≥–Њ —П–≤–ї—П—О—В—Б—П –Љ–∞–ї—Л–µ –∞–љ–Њ–Љ–∞–ї–Є–Є —Б–µ—А–і—Ж–∞ (–Ь–Р–°) [6,7]. –Ъ –Ь–Р–° –Њ—В–љ–Њ—Б—П—В—Б—П –њ—А–Њ–ї–∞–њ—Б—Л –Ї–ї–∞–њ–∞–љ–Њ–≤: —В—А–Є–Ї—Г—Б–њ–Є–і–∞–ї—М–љ–Њ–≥–Њ, –∞–Њ—А—В–∞–ї—М–љ–Њ–≥–Њ, –ї–µ–≥–Њ—З–љ–Њ–є –∞—А—В–µ—А–Є–Є; –∞–љ–µ–≤—А–Є–Ј–Љ–∞ –Љ–µ–ґ–њ—А–µ–і—Б–µ—А–і–љ–Њ–є –њ–µ—А–µ–≥–Њ—А–Њ–і–Ї–Є; —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А—Г—О—Й–µ–µ –Њ–≤–∞–ї—М–љ–Њ–µ –Њ–Ї–љ–Њ; –∞—Б–Є–Љ–Љ–µ—В—А–Є—П —В—А–Є–Ї—Г—Б–њ–Є–і–∞–ї—М–љ–Њ–≥–Њ –Ї–ї–∞–њ–∞–љ–∞; –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л–µ –∞–љ–Њ–Љ–∞–ї—М–љ–Њ —А–∞–Ј–≤–Є—В—Л–µ —Е–Њ—А–і—Л (–Р–†–•) [6]. –Ь–Р–° —П–≤–ї—П—О—В—Б—П –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Њ—Б–љ–Њ–≤–Њ–є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Б–µ—А–і–µ—З–љ–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є –Є —З–∞—Б—В–Њ —Б–Њ—З–µ—В–∞—О—В—Б—П —Б —Н–ї–µ–Ї—В—А–Є—З–µ—Б–Ї–Њ–є –љ–µ—Б—В–∞–±–Є–ї—М–љ–Њ—Б—В—М—О –Љ–Є–Њ–Ї–∞—А–і–∞, –њ—А–Њ—П–≤–ї—П—О—Й–µ–є—Б—П —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є —А–Є—В–Љ–∞ [6]. –Ю—Б–љ–Њ–≤–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –љ–∞—А—Г—И–µ–љ–Є—П —А–Є—В–Љ–∞ –њ—А–Є –Ф–°–Ґ —Б–ї–µ–і—Г—О—Й–Є–µ: –љ–∞—А—Г—И–µ–љ–Є—П –∞–≤—В–Њ–Љ–∞—В–Є–Ј–Љ–∞, —В—А–Є–≥–≥–µ—А–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М, Re-entry. –Я—А–µ–і—А–∞—Б–њ–Њ–ї–∞–≥–∞—О—Й–Є–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є –∞—А–Є—В–Љ–Њ–≥–µ–љ–µ–Ј–∞ —П–≤–ї—П—О—В—Б—П: –љ–µ–њ–Њ–ї–љ–Њ—Ж–µ–љ–љ–Њ—Б—В—М –≤–љ–µ–Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ –Љ–∞—В—А–Є–Ї—Б–∞; –і–Є—Б—Д—Г–љ–Ї—Ж–Є—П –Љ–Є–Њ–Ї–∞—А–і–∞ –Ы–Ц; —Б–Њ—Б—В–Њ—П–љ–Є–µ –Ї–ї–∞–њ–∞–љ–љ–Њ-—Е–Њ—А–і–∞–ї—М–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞ (–Я–Ь–Ъ, –Ф–•–Ы–Ц, –Љ–Є–Ї—Б–Њ–Љ–∞—В–Њ–Ј–љ–∞—П –і–µ–≥–µ–љ–µ—А–∞—Ж–Є—П —Б—В–≤–Њ—А–Њ–Ї, –Љ–Є—В—А–∞–ї—М–љ–∞—П —А–µ–≥—Г—А–≥–Є—В–∞—Ж–Є—П); –Љ—Л—И–µ—З–љ—Л–µ –Љ–Њ—Б—В–Є–Ї–Є; –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ –њ—Г—В–Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Є–Љ–њ—Г–ї—М—Б–∞; —Н–ї–µ–Ї—В—А–Њ–ї–Є—В–љ—Л–µ —Б–і–≤–Є–≥–Є (–≥–Є–њ–Њ–Љ–∞–≥–љ–Є–µ–Љ–Є—П); –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ—Л–µ —Б–і–≤–Є–≥–Є (–≥–Є–њ–µ—А–њ—А–Њ–ї–∞–Ї—В–Є–љ–µ–Љ–Є—П) [6,7].
–Ф–Є—Б–њ–ї–∞—Б—В–Є—З–µ—Б–Ї–Њ–µ —Б–µ—А–і—Ж–µ –ї–µ–ґ–Є—В –≤ –Њ—Б–љ–Њ–≤–µ –Љ–љ–Њ–≥–Є—Е —Б–ї—Г—З–∞–µ–≤ –≤–љ–µ–Ј–∞–њ–љ–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є —Б–Љ–µ—А—В–Є, –њ—А–Є—З–Є–љ–∞–Љ–Є –Ї–Њ—В–Њ—А–Њ–є —П–≤–ї—П—О—В—Б—П —Д–∞—В–∞–ї—М–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П —А–Є—В–Љ–∞ –Є –њ—А–Њ–≤–Њ–і–Є–Љ–Њ—Б—В–Є, —А–∞–Ј—А—Л–≤—Л –Є –∞–љ–µ–≤—А–Є–Ј–Љ—Л –∞–Њ—А—В—Л, –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е –Є –Љ–Њ–Ј–≥–Њ–≤—Л—Е –∞—А—В–µ—А–Є–є [6].
–°–∞–Љ—Л–Љ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є–µ–Љ –і–Є—Б–њ–ї–∞—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–µ—А–і—Ж–∞ —П–≤–ї—П–µ—В—Б—П –њ—А–Њ–ї–∞–±–Є—А–Њ–≤–∞–љ–Є–µ –Љ–Є—В—А–∞–ї—М–љ–Њ–≥–Њ –Ї–ї–∞–њ–∞–љ–∞. –Я—А–Њ–≥–љ–Њ–Ј –і–ї—П –±–Њ–ї—М–љ–Њ–≥–Њ —Б –Я–Ь–Ъ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П —Б—В–µ–њ–µ–љ—М—О –Љ–Є—В—А–∞–ї—М–љ–Њ–є —А–µ–≥—Г—А–≥–Є—В–∞—Ж–Є–Є [7]. –У–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–∞—П –Љ–Є—В—А–∞–ї—М–љ–∞—П —А–µ–≥—Г—А–≥–Є—В–∞—Ж–Є—П –Њ–±—Л—З–љ–Њ —Б–≤—П–Ј–∞–љ–∞ —Б –Љ–Є–Ї—Б–Њ–Љ–∞—В–Њ–Ј–љ—Л–Љ –њ–µ—А–µ—А–Њ–ґ–і–µ–љ–Є–µ–Љ —Б—В—А—Г–Ї—В—Г—А –Ї–ї–∞–њ–∞–љ–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞ –Є —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –і–Є—Д—Д—Г–Ј–љ—Л–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ —Д–Є–±—А–Њ–Ј–љ–Њ–≥–Њ —Б–ї–Њ—П, –і–µ—Б—В—А—Г–Ї—Ж–Є–µ–є –Є —Д—А–∞–≥–Љ–µ–љ—В–∞—Ж–Є–µ–є –Ї–Њ–ї–ї–∞–≥–µ–љ–Њ–≤—Л—Е –Є —Н–ї–∞—Б—В–Є—З–µ—Б–Ї–Є—Е –≤–Њ–ї–Њ–Ї–Њ–љ, —Г—Б–Є–ї–µ–љ–љ—Л–Љ –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ–Љ –≥–ї–Є–Ї–Њ–Ј–∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–∞–љ–Њ–≤ –≤–Њ –≤–љ–µ–Ї–ї–µ—В–Њ—З–љ–Њ–Љ –Љ–∞—В—А–Є–Ї—Б–µ [7]. –£ –њ–Њ–ї–Њ–≤–Є–љ—Л –±–Њ–ї—М–љ—Л—Е —Б –Я–Ь–Ъ –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Є –≥–Є—Б—В–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ –Љ–Є–Ї—Б–Њ–Љ–∞—В–Њ–Ј–љ–Њ–µ –њ–µ—А–µ—А–Њ–ґ–і–µ–љ–Є–µ –њ—А–Њ–≤–Њ–і—П—Й–µ–є —Б–Є—Б—В–µ–Љ—Л —Б–µ—А–і—Ж–∞, –∞ —В–∞–Ї–ґ–µ –≤–љ—Г—В—А–Є—Б–µ—А–і–µ—З–љ—Л—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ. –І–∞—Б—В–Њ –≤—Л—П–≤–ї—П–µ—В—Б—П –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М –Я–Ь–Ъ —Б –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є —А–Є—В–Љ–∞ —Б–µ—А–і—Ж–∞. –І–∞—Б—В–Њ—В–∞ –≤—Л—П–≤–ї–µ–љ–Є—П –ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤—Л—Е —Н–Ї—Б—В—А–∞—Б–Є—Б—В–Њ–ї –Ї–Њ–ї–µ–±–ї–µ—В—Б—П –Њ—В 18% –і–Њ 91%, –љ–∞–і–ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤—Л—Е —Н–Ї—Б—В—А–∞—Б–Є—Б—В–Њ–ївАФ –≤ –њ—А–µ–і–µ–ї–∞—Е
–І–∞—Б—В–Њ –њ—А–Є –°–Ф–° –≤—Л—П–≤–ї—П—О—В—Б—П –∞–љ–Њ–Љ–∞–ї—М–љ–Њ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л–µ —Е–Њ—А–і—Л (12%). –І–∞—Б—В–Њ—В–∞ –≤—Л—П–≤–ї–µ–љ–Є—П –Р–†–• –Ї–Њ–ї–µ–±–ї–µ—В—Б—П –Њ—В 2,5 –і–Њ 95% [7]. –Т —В–Ї–∞–љ—П—Е, —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л—Е –≤ —Г—З–∞—Б—В–Ї–∞—Е –њ—А–Є–Ї—А–µ–њ–ї–µ–љ–Є—П —Е–Њ—А–і—Л, –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ–Њ—Б—В–Њ—П–љ–љ–Њ–є —В—А–∞–Ї—Ж–Є–Є –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –љ–∞—А—Г—И–µ–љ–Є–µ —А–µ–≥–Є–Њ–љ–∞—А–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –Є —Д–Њ—А–Љ–Є—А—Г—О—В—Б—П –Ј–Њ–љ—Л —Д–Є–±—А–Њ–Ј–∞. –Я—А–Є –љ–∞–ї–Є—З–Є–Є –∞–љ–Њ–Љ–∞–ї—М–љ–Њ–≥–Њ –њ–Њ–њ–µ—А–µ—З–љ–Њ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ–≥–Њ —В—П–ґ–∞ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П —В—Г—А–±—Г–ї–µ–љ—В–љ—Л–є –≤–љ—Г—В—А–Є—Б–µ—А–і–µ—З–љ—Л–є –Ї—А–Њ–≤–Њ—В–Њ–Ї, –Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є–є –њ–Њ–≤—А–µ–ґ–і–∞—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ —В–Ї–∞–љ–Є —Б–∞–Љ–Њ–є —Е–Њ—А–і—Л –Є —Н–љ–і–Њ–Ї–∞—А–і. –Ю—Б–љ–Њ–≤–љ–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Р–†–• –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ —В–Њ–Љ, —З—В–Њ –Њ–љ–Є —П–≤–ї—П—О—В—Б—П –Њ–і–љ–Њ–є –Є–Ј –≤–Њ–Ј–Љ–Њ–ґ–љ—Л—Е –њ—А–Є—З–Є–љ –∞—А–Є—В–Љ–Є–є, —В–∞–Ї –Ї–∞–Ї –Љ–Њ–≥—Г—В —Б–Њ–і–µ—А–ґ–∞—В—М –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ –њ—Г—В–Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Є–Љ–њ—Г–ї—М—Б–∞ (–Ї–ї–µ—В–Ї–Є –Я—Г—А–Ї–Є–љ—М–µ). –Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –њ—А–Є –Р–†–• –≤—Л—П–≤–ї—П—О—В—Б—П –љ–∞–і–ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤–∞—П –Є –ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤–∞—П —Н–Ї—Б—В—А–∞—Б–Є—Б—В–Њ–ї–Є—П. –Я—А–Њ–і–Њ–ї—М–љ–Њ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л–µ –Р–†–• —З–∞—Й–µ —Б–Њ—З–µ—В–∞—О—В—Б—П —Б –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є —А–Є—В–Љ–∞ —Б–µ—А–і—Ж–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–Њ–њ–µ—А–µ—З–љ—Л–Љ–Є –Є –і–Є–∞–≥–Њ–љ–∞–ї—М–љ—Л–Љ–Є —Е–Њ—А–і–∞–Љ–Є [6].
–¶–µ–ї—М —А–∞–±–Њ—В—Л вАФ –∞–љ–∞–ї–Є–Ј –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є —А–Є—В–Љ–∞ –Є –њ—А–Њ–≤–Њ–і–Є–Љ–Њ—Б—В–Є –Є –Љ–∞–ї—Л—Е –∞–љ–Њ–Љ–∞–ї–Є–є —Б–µ—А–і—Ж–∞ –њ—А–Є –≥–Є–њ–µ—А—В—А–Њ—Д–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А–і–Є–Њ–Љ–Є–Њ–њ–∞—В–Є–Є.
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –≤ —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤–Ї–ї—О—З–µ–љ—Л 42 –њ–∞—Ж–Є–µ–љ—В–∞ —Б –У–Ъ–Ь–Я (–і–Є–∞–≥–љ–Њ–Ј —Г—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–ї—Б—П —Б–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ –њ–Њ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Є –ї–µ—З–µ–љ–Є—О –±–Њ–ї—М–љ—Л—Е –У–Ъ–Ь–Я). –Ш–Ј—Г—З–µ–љ—Л —А–µ–Ј—Г–ї—М—В–∞—В—Л –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ, —Н—Е–Њ–Ї–∞—А–і–Є–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Њ–≥–Њ, —Н–ї–µ–Ї—В—А–Њ–Ї–∞—А–і–Є–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є —Б—Г—В–Њ—З–љ–Њ–≥–Њ —Е–Њ–ї—В–µ—А–Њ–≤—Б–Ї–Њ–≥–Њ –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є—П –≠–Ъ–У —Г –і–∞–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤. —Г –і–∞–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј –њ—А–Њ–≤–Њ–і–Є–ї—Б—П –њ—А–Є –њ–Њ–Љ–Њ—Й–Є –њ—А–Њ–≥—А–∞–Љ–Љ—Л Statistica 10.0, –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ–Є —А–∞–Ј–ї–Є—З–Є—П —Б—З–Є—В–∞–ї–Є—Б—М –њ—А–Є p <0,05.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Е –Њ–±—Б—Г–ґ–і–µ–љ–Є–µ. –Ш–Ј 42, –≤–Њ—И–µ–і—И–Є—Е –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –≥—А—Г–њ–њ—Г —Б –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–є —Д–Њ—А–Љ–Њ–є –≥–Є–њ–µ—А—В—А–Њ—Д–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А–і–Є–Њ–Љ–Є–Њ–њ–∞—В–Є–Є (–Ю–У–Ъ–Ь–Я) —Б–Њ—Б—В–∞–≤–Є–ї–Є 17, —Г –Ї–Њ—В–Њ—А—Л—Е –≥—А–∞–і–Є–µ–љ—В –і–∞–≤–ї–µ–љ–Є—П –≤ –≤—Л–≤–Њ–і–љ–Њ–Љ —В—А–∞–Ї—В–µ (–Т–Ґ) –Ы–Ц –њ—А–µ–≤—Л—И–∞–ї 30 –Љ–Љ —А—В —Б—В., –≤ –≥—А—Г–њ–њ—Г —Б –љ–µ–Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–є —Д–Њ—А–Љ–Њ–є –У–Ъ–Ь–Я (–Э–У–Ъ–Ь–Я) –≤–Њ—И–ї–Є 25 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Б –≥—А–∞–і–Є–µ–љ—В–Њ–Љ –і–∞–≤–ї–µ–љ–Є—П –≤ –Т–Ґ –Ы–Ц <30 –Љ–Љ —А—В —Б—В. –Ь–µ–і–Є–∞–љ–∞ –≤–Њ–Ј—А–∞—Б—В–∞ –њ–Њ—Б—В—А–∞–і–∞–≤—И–Є—Е –≤ –≥—А—Г–њ–њ–µ —Б –Ю–У–Ъ–Ь–Я —Б–Њ—Б—В–∞–≤–Є–ї–∞ –Ь–µ(95% –Ф–Ш) = 50
–Т –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–Љ –Ї–Њ–љ—В–Є–љ–≥–µ–љ—В–µ –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –≤—Б—В—А–µ—З–∞–ї—Б—П –њ—А–Њ–ї–∞–њ—Б –Љ–Є—В—А–∞–ї—М–љ–Њ–≥–Њ –Ї–ї–∞–њ–∞–љ–∞, (64,3%) –Є –∞–љ–Њ–Љ–∞–ї—М–љ–Њ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–∞—П —Е–Њ—А–і–∞ –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ (–Ы–Ц) (21,4%). –Ф–µ—Д–µ–Ї—В –Љ–µ–ґ–њ—А–µ–і—Б–µ—А–і–љ–Њ–є –њ–µ—А–µ–≥–Њ—А–Њ–і–Є (–Ф–Ь–Я–Я) –Є –Љ–Є–Ї—Б–Њ–Љ–∞—В–Њ–Ј —Б—В–≤–Њ—А–Њ–Ї –Ь–Ъ –љ–∞–±–ї—О–і–∞–ї–Є—Б—М –≤ 11,9% —Б–ї—Г—З–∞–µ–≤ –Ї–∞–ґ–і—Л–є. –Ю—В–Ї—А—Л—В–Њ–µ –Њ–≤–∞–ї—М–љ–Њ–µ –Њ–Ї–љ–Њ –≤—Л—П–≤–ї–µ–љ–Њ —Г 9,5% –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Њ–ї–∞–њ—Б —В—А–Є–Ї—Г—Б–њ–Є–і–∞–ї—М–љ–Њ–≥–Њ –Ї–ї–∞–њ–∞–љ–∞ –Є —В—А–∞–±–µ–Ї—Г–ї—П—А–љ–Њ—Б—В—М –≤–µ—А—Е—Г—И–Ї–Є –њ—А–∞–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ (–Я–Ц) —Г 7,1%. –Ф–Є–ї–∞—В–∞—Ж–Є—П –Њ—В–≤–µ—А—Б—В–Є—П —В—А–Є–Ї—Г—Б–њ–Є–і–∞–ї—М–љ–Њ–≥–Њ –Ї–ї–∞–њ–∞–љ–∞, —Б–µ—В—М Chiari, –і–µ—Д–µ–Ї—В –Љ–µ–ґ–ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤–Њ–є –њ–µ—А–µ–≥–Њ—А–Њ–і–Ї–Є (–Ф–Ь–Ц–Я) –≤—Л—П–≤–ї–µ–љ—Л –≤ 2,4% —Б–ї—Г—З–∞–µ–≤.
–Т –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ—А–µ–Њ–±–ї–∞–і–∞–ї–Є –љ–∞–і–ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤—Л–µ (–≤—Л—П–≤–ї–µ–љ—Л —Г 22 (52,4%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤) –Є –ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤—Л–µ (–≤—Л—П–≤–ї–µ–љ—Л —Г 18 (42,9%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤) —Н–Ї—Б—В—А–∞—Б–Є—Б—В–Њ–ї—Л. –Ь–Є–≥—А–∞—Ж–Є—П –≤–Њ–і–Є—В–µ–ї—П —А–Є—В–Љ–∞ –±—Л–ї–∞ –Њ–±–љ–∞—А—Г–ґ–µ–љ–∞ —Г 2 (4,8%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –°–Є–љ–і—А–Њ–Љ WPW, —Д–Є–±—А–Є–ї–ї—П—Ж–Є—П –њ—А–µ–і—Б–µ—А–і–Є–є, —В—А–µ–њ–µ—В–∞–љ–Є–µ –њ—А–µ–і—Б–µ—А–і–Є–є, –њ–Њ–ї–љ–∞—П –±–ї–Њ–Ї–∞–і–∞ –ї–µ–≤–Њ–є –љ–Њ–ґ–Ї–Є –њ—Г—З–Ї–∞ –У–Є—Б–∞, –љ–µ–њ–Њ–ї–љ–∞—П –Р–Т-–±–ї–Њ–Ї–∞–і–∞ II —Б—В–µ–њ–µ–љ–Є –Ь–Њ–±–Є—В—Ж 1 –≤—Б—В—А–µ—З–∞–ї–Є—Б—М –њ–Њ 2,4% —Б–ї—Г—З–∞–µ–≤.
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–Њ –≤–ї–Є—П–љ–Є–µ –Ь–Р–° –љ–∞ —А–∞–Ј–≤–Є—В–Є–µ –љ–∞—А—Г—И–µ–љ–Є–є —А–Є—В–Љ–∞ –≤ –≥—А—Г–њ–њ–∞—Е —Б –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–є –Є –љ–µ–Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–є —Д–Њ—А–Љ–Њ–є –≥–Є–њ–µ—А—В—А–Њ—Д–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А–і–Є–Њ–Љ–Є–Њ–њ–∞—В–Є–Є (—В–∞–±–ї–Є—Ж–∞ 1).
–Ґ–∞–±–ї–Є—Ж–∞ 1
–°–Њ—З–µ—В–∞–љ–Є–µ –Ь–Р–° –Є –љ–∞—А—Г—И–µ–љ–Є–є —А–Є—В–Љ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –У–Ъ–Ь–Я
| –Я—А–Є–Ј–љ–∞–Ї | –Я–∞—Ж–Є–µ–љ—В—Л —Б –Ю–У–Ъ–Ь–Я (n=17), –∞–±—Б. —З–Є—Б–ї–Њ (%) | –Я–∞—Ж–Є–µ–љ—В—Л —Б –Э–У–Ъ–Ь–Я (n=25), –∞–±—Б. —З–Є—Б–ї–Њ (%) | ||||
| –Ь–Р–° (n=12) | –С–µ–Ј –Ь–Р–° (n=5) | —А | –Ь–Р–° (n=22) | –С–µ–Ј –Ь–Р–° (n=3) | —А | |
| –° –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є —А–Є—В–Љ–∞ | 10 (58,8%) | 5 (29,4%) | 0,89 | 20 (80%) | 3 (12%) | 0,74 |
| –Я–Ь–Ъ (n=11) | –С–µ–Ј –Я–Ь–Ъ (n=6) | p | –Я–Ь–Ъ (n=19) | –С–µ–Ј –Я–Ь–Ъ (n=6) | p | |
| –° –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є —А–Є—В–Љ–∞ | 8 (47%) | 6 (35,2%) | 0,48 | 14 (56%) | 5 (20%) | 0,86 |
–Т –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–Љ –Ї–Њ–љ—В–Є–љ–≥–µ–љ—В–µ –≤ –≥—А—Г–њ–њ–µ —Б –Ю–У–Ъ–Ь–Я –љ–∞—А—Г—И–µ–љ–Є—П —А–Є—В–Љ–∞ –±—Л–ї–Є –≤—Л—П–≤–ї–µ–љ—Л —Г 24,9% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј –Ь–Р–°, –∞ –њ—А–Є –љ–∞–ї–Є—З–Є–Є –љ–∞—А—Г—И–µ–љ–Є–є –∞—А—Е–Є—В–µ–Ї—В–Њ–љ–Є–Ї–Є вАФ —Г 58,8%. –Т –≥—А—Г–њ–њ–µ —Б –Э–У–Ъ–Ь–Я –љ–∞—А—Г—И–µ–љ–Є—П —А–Є—В–Љ–∞ –≤—Б—В—А–µ—З–∞–ї–Є—Б—М —Г 12% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј –Ь–Р–° –Є —Г 80% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Љ–∞–ї—Л–Љ–Є –∞–љ–Њ–Љ–∞–ї–Є—П–Љ–Є —Б–µ—А–і—Ж–∞. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–У–Ъ–Ь–Я, –Є–Љ–µ—О—Й–Є—Е –Я–Ь–Ъ, –∞—А–Є—В–Љ–Є–Є –≤—Л—П–≤–ї–µ–љ—Л —Г 47% –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –°—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –і–∞–љ–љ–Њ–є –≥—А—Г–њ–њ—Л, —Г –Ї–Њ—В–Њ—А—Л—Е –љ–µ –±—Л–ї –≤—Л—П–≤–ї–µ–љ –Я–Ь–Ъ –љ–∞—А—Г—И–µ–љ–Є—П —А–Є—В–Љ–∞ –≤—Л—П–≤–ї–µ–љ—Л —Г 35,2% –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Т –≥—А—Г–њ–њ–µ —Б –Э–У–Ъ–Ь–Я –њ—А–Є –љ–∞–ї–Є—З–Є–Є –Я–Ь–Ъ –љ–∞—А—Г—И–µ–љ–Є—П —А–Є—В–Љ–∞ –≤—Л—П–≤–ї–µ–љ—Л —Г 56% –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –∞ –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –Я–Ь–Ъ вАФ —Г 20%. (—А–Є—Б—Г–љ–Њ–Ї 1).
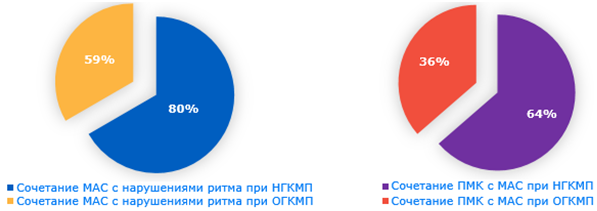
–†–Є—Б.1. –°–Њ—З–µ—В–∞–љ–Є–µ –∞—А–Є—В–Љ–Є–є —Б –Ь–Р–° –Є –Я–Ь–Ъ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –У–Ъ–Ь–Я
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —А–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –љ–∞—А—Г—И–µ–љ–Є—П —А–Є—В–Љ–∞ —З–∞—Й–µ –≤—Б—В—А–µ—З–∞–ї–Є—Б—М –њ—А–Є –љ–∞–ї–Є—З–Є–Є –Љ–∞–ї—Л—Е –∞–љ–Њ–Љ–∞–ї–Є–є —Б–µ—А–і—Ж–∞. –Т –≥—А—Г–њ–њ–µ —Б –Э–У–Ъ–Ь–Я —Б–Њ—З–µ—В–∞–љ–Є–µ –Ь–Р–° –Є –∞—А–Є—В–Љ–Є–є –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Г 80%, –∞ –≤ –≥—А—Г–њ–њ–µ —Б –Ю–У–Ъ–Ь–Я —Г 58,8% –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Я–Ь–Ъ —Б–Њ—З–µ—В–∞–ї—Б—П —Б –Ь–Р–° —Г 47% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–У–Ъ–Ь–Я –Є —Г 56% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Э–У–Ъ–Ь–Я. –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –≤–Њ –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –Ь–Р–° –Є –љ–∞—А—Г—И–µ–љ–Є–є —А–Є—В–Љ–∞ –≤ –≥—А—Г–њ–њ–∞—Е —Б –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–є –Є –љ–µ–Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–є —Д–Њ—А–Љ–Њ–є –≥–Є–њ–µ—А—В—А–Њ—Д–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А–і–Є–Њ–Љ–Є–Њ–њ–∞—В–Є–Є –љ–µ –≤—Л—П–≤–ї–µ–љ–Њ.
–Э–∞ –і–∞–љ–љ—Л–є –Љ–Њ–Љ–µ–љ—В –Њ—В—Б—Г—В—Б—В–≤—Г—О—В –Њ–і–љ–Њ–Ј–љ–∞—З–љ—Л–µ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є–µ –і–∞–љ–љ—Л–µ –Њ —Б–Њ—З–µ—В–∞–љ–Є–Є –У–Ъ–Ь–Я –Є –Ь–Р–°. –Я–Њ –і–∞–љ–љ—Л–Љ –Ѓ. –Э. –С–µ–ї–µ–љ–Ї–Њ–≤–∞, –Х. –Т. –Я—А–Є–≤–∞–ї–Њ–≤–Њ–є, –Т. –Ѓ. –Ъ–∞–њ–ї—Г–љ–Њ–≤–Њ–є –Є –і—А. –У–Ъ–Ь–Я –≤ 50% –љ–∞–±–ї—О–і–µ–љ–Є–є —Б–Њ—З–µ—В–∞–µ—В—Б—П —Б –∞–љ–Њ–Љ–∞–ї–Є—П–Љ–Є —А–∞–Ј–≤–Є—В–Є—П, –Ї–∞–Ї –Ї–∞—А–і–Є–∞–ї—М–љ—Л–Љ–Є, —В–∞–Ї –Є –≤–љ–µ–Ї–∞—А–і–Є–∞–ї—М–љ—Л–Љ–Є [4]. –Т 17% —Б–ї—Г—З–∞–µ–≤ –Њ—В–Љ–µ—З–µ–љ–Њ —Б–Њ—З–µ—В–∞–љ–Є–µ –У–Ъ–Ь–Я —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –≤–∞—А–Є–∞–љ—В–∞–Љ–Є –і–Є—Б–њ–ї–∞–Ј–Є–Є —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є. –Ю—Ж–µ–љ–Ї–∞ —Б—В—А—Г–Ї—В—Г—А—Л –≤—Л—П–≤–ї–µ–љ–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Г –љ–∞–±–ї—О–і–∞–µ–Љ—Л—Е –±–Њ–ї—М–љ—Л—Е –≤—Л—П–≤–Є–ї–∞ —Б–ї–µ–і—Г—О—Й–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є: –Я–Ь–Ъ вАФ 6,3%, –њ—А–Њ–ї–∞–њ—Б —В—А–Є–Ї—Г—Б–њ–Є–і–∞–ї—М–љ–Њ–≥–Њ –Ї–ї–∞–њ–∞–љ–∞ вАФ 2,7%, –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ —Е–Њ—А–і—Л вАФ 4,5% –і–≤—Г—Е—Б—В–≤–Њ—А—З–∞—В—Л–є –∞–Њ—А—В–∞–ї—М–љ—Л–є –Ї–ї–∞–њ–∞–љ вАФ 1,8%, –њ–Њ–≤—Л—И–µ–љ–љ–∞—П —В—А–∞–±–µ–Ї—Г–ї—П—А–љ–Њ—Б—В—М –Ы–Ц вАФ 3,6%, –∞–љ–µ–≤—А–Є–Ј–Љ–∞ –Ь–Я–Я вАФ 3,6%, –і–µ—Д–µ–Ї—В –Љ–µ–Љ–±—А–∞–љ–Њ–Ј–љ–Њ–є —З–∞—Б—В–Є –Ь–Ц–Я вАФ 1,8% [4]. –°–Њ–≥–ї–∞—Б–љ–Њ –і–∞–љ–љ—Л–Љ –§.–Ґ. –Р–≥–µ–µ–≤–∞ –Є —Б–Њ–∞–≤—В. —Г 96,5% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –У–Ъ–Ь–Я —А–µ–≥–Є—Б—В—А–Є—А—Г—О—В—Б—П —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П —А–Є—В–Љ–∞ —Б–µ—А–і—Ж–∞: –Ц–≠ –≤ 81,4%, —Н–њ–Є–Ј–Њ–і—Л –љ–µ—Г—Б—В–Њ–є—З–Є–≤–Њ–є –Ц–Ґ –≤ 23%, –Э–Ц–≠ –≤ 72,8%, —Н–њ–Є–Ј–Њ–і—Л –Э–Ц–Ґ –≤ 31,8%, –њ–Њ—Б—В–Њ—П–љ–љ–∞—П —Д–Њ—А–Љ–∞ –Ь–Р –≤ 6,9%, –њ–∞—А–Њ–Ї—Б–Є–Ј–Љ—Л –Ь–Р –≤ 2,7% —Б–ї—Г—З–∞–µ–≤ [1]. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Ѓ.–Э. –С–µ–ї–µ–љ–Ї–Њ–≤–∞ –Є —Б–Њ–∞–≤. —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–Є –Љ–љ–Њ–≥–Њ–ї–µ—В–љ–µ–Љ –љ–∞–±–ї—О–і–µ–љ–Є–Є –Ј–∞ –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є —Б –У–Ъ–Ь–Я —Г–Ї–∞–Ј—Л–≤–∞—О—В –љ–∞ —Г—Б–Є–ї–µ–љ–Є–µ –Є —Г–њ–Њ—А—Б—В–≤–Њ –∞—А–Є—В–Љ–Є–є –њ—А–Є —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Ь–Р–° –≤ –њ—А–Њ–≥—А–∞–Љ–Љ–µ –°–Ф–°–Ґ [4].
–Т—Л–≤–Њ–і—Л: –У–Ъ–Ь–Я —З–∞—Б—В–Њ —Б–Њ—З–µ—В–∞–µ—В—Б—П —Б —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –љ–µ–і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–є –і–Є—Б–њ–ї–∞–Ј–Є–Є —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є, –Њ–і–љ–Є–Љ –Є–Ј –њ—А–Њ—П–≤–ї–µ–љ–Є–є –Ї–Њ—В–Њ—А–Њ–≥–Њ —П–≤–ї—П–µ—В—Б—П —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –Љ–∞–ї—Л—Е –∞–љ–Њ–Љ–∞–ї–Є–є —Б–µ—А–і—Ж–∞, —З—В–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –љ–∞—А—Г—И–µ–љ–Є–µ–Љ –∞—А—Е–Є—В–µ–Ї—В–Њ–љ–Є–Ї–Є –Љ–Є–Њ–Ї–∞—А–і–∞ –Є –µ–≥–Њ —Н–ї–µ–Ї—В—А–Є—З–µ—Б–Ї–Њ–є –љ–µ—Б—В–∞–±–Є–ї—М–љ–Њ—Б—В—М—О, —П–≤–ї—П—О—Й–Є–є—Б—П —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –∞—А–Є—В–Љ–Є–є —Б–µ—А–і—Ж–∞, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є –ґ–Є–Ј–љ–µ—Г–≥—А–Њ–ґ–∞—О—Й–Є—Е, —З—В–Њ –≤–∞–ґ–љ–Њ –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –У–Ъ–Ь–Я. –Т –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–Љ –Ї–Њ–љ—В–Є–љ–≥–µ–љ—В–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –У–Ъ–Ь–Я –љ–∞—А—Г—И–µ–љ–Є—П —А–Є—В–Љ–∞ —З–∞—Й–µ –≤—Б—В—А–µ—З–∞–ї–Є—Б—М –њ—А–Є –љ–∞–ї–Є—З–Є–Є –Љ–∞–ї—Л—Е –∞–љ–Њ–Љ–∞–ї–Є–є —Б–µ—А–і—Ж–∞. –Т –≥—А—Г–њ–њ–µ —Б –Э–У–Ъ–Ь–Я —Б–Њ—З–µ—В–∞–љ–Є–µ –Ь–Р–° –Є –∞—А–Є—В–Љ–Є–є –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Г 80%, –∞ –≤ –≥—А—Г–њ–њ–µ —Б –Ю–У–Ъ–Ь–Я —Г 58,8% –њ–∞—Ж–Є–µ–љ—В–Њ–≤.
–Ы–Є—В–µ—А–∞—В—Г—А–∞
- –Р–≥–µ–µ–≤, –§.–Ґ., –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Є –ї–µ—З–µ–љ–Є—О –Ї–∞—А–і–Є–Њ–Љ–Є–Њ–њ–∞—В–Є–є (–≥–Є–њ–µ—А—В—А–Њ—Д–Є—З–µ—Б–Ї–∞—П) / –§. –Ґ. –Р–≥–µ–µ–≤, –°. –Р. –У–∞–±—А—Г—Б–µ–љ–Ї–Њ, –Р. –Ѓ. –Я–Њ—Б—В–љ–Њ–≤ –Є –і—А. // –Х–≤—А–∞–Ј–Є–є—Б–Ї–Є–є –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї. вАФ 2014. вАФ вДЦ 3. вАФ –°. 4 вАФ 23.
- –С–Њ–Ї–µ—А–Є—П –Ы. –С., –У–Є–њ–µ—А—В—А–Њ—Д–Є—З–µ—Б–Ї–∞—П –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–∞—П –Ї–∞—А–і–Є–Њ–Љ–Є–Њ–њ–∞—В–Є—П / –Ы. –С. –С–Њ–Ї–µ—А–Є—П // –Р–љ–љ–∞–ї—Л —Е–Є—А—Г—А–≥–Є–Є. 2013. вАФ вДЦ 5. –°.
5-14. - –С–Њ–Ї–µ—А–Є—П –Ы. –С., –Р—А–Є—В–Љ–Њ–≥–µ–љ–љ—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –≥–Є–њ–µ—А—В—А–Њ—Д–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А–і–Є–Њ–Є–Њ–њ–∞—В–Є–Є / –Ы. –Р. –С–Њ–Ї–µ—А–Є—П, –Ь. –Ш. –С–µ—А—Б–µ–љ—С–≤–∞, –Ф. –Р. –Ь–∞–ї–µ–љ–Ї–Њ–≤ // –Р–љ–љ–∞–ї—Л –∞—А–Є—В–Љ–Њ–ї–Њ–≥–Є–Є. 2010. вАФ вДЦ 3. C.
62-69. - –С–µ–ї–µ–љ–Ї–Њ–≤, –Ѓ. –Э., –У–Є–њ–µ—А—В—А–Њ—Д–Є—З–µ—Б–Ї–∞—П –Ї–∞—А–і–Є–Њ–Љ–Є–Њ–њ–∞—В–Є—П –Є —Б–Є–љ–і—А–Њ–Љ –і–Є—Б–њ–ї–∞–Ј–Є–Є —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є, –≤–∞—А–Є–∞–љ—В—Л —Б–Њ—З–µ—В–∞–љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є / –Ѓ. –Э. –С–µ–ї–µ–љ–Ї–Њ–≤, –Х. –Т. –Я—А–Є–≤–∞–ї–Њ–≤–∞, –Т. –Ѓ. –Ъ–∞–њ–ї—Г–љ–Њ–≤–∞ –Є –і—А. // –†–∞—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є—П –≤ –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є–Є. вАФ 2016. вАФ –Ґ. 12. вДЦ 5. вАФ –°. 522 вАФ 527.
- –Ю—Б–Є–µ–≤ –Р.–У., –У–Є–њ–µ—А—В—А–Њ—Д–Є—З–µ—Б–Ї–∞—П –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–∞—П –Ї–∞—А–і–Є–Њ–Љ–Є–Њ–њ–∞—В–Є—П / –Р. –У. –Ю—Б–Є–µ–≤, –†. –Р. –Э–∞–є–і–µ–љ–Њ–≤, –Х. –Ш. –Ъ—А–µ—В–Њ–≤ –Є –і—А. // –Р–ї—М–Љ–∞–љ–∞—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Л. вАФ 2015. вДЦ 38. вАФ –°.
95вАУ104. - –Ь–∞—Б–ї–Њ–≤—Б–Ї–∞—П –Ь. –Т., –Э–µ–і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞–љ–љ–∞—П –і–Є—Б–њ–ї–∞–Ј–Є—П —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є –Є –Љ–∞–ї—Л–µ –∞–љ–Њ–Љ–∞–ї–Є–Є —Б–µ—А–і—Ж–∞ –Ї–∞–Ї –њ—А–µ–і–Є–Ї—В–Њ—А —А–∞–Ј–≤–Є—В–Є—П –љ–∞—А—Г—И–µ–љ–Є–є —А–Є—В–Љ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ—М—О —Б–µ—А–і—Ж–∞ / –Ь. –Т. –Ь–∞—Б–ї–Њ–≤—Б–Ї–∞—П, –Ы–Њ–ї–ї–Є–љ–Є –Т. –Р. // –Т–µ—Б—В–љ–Є–Ї –Т–У–Ь–£ вИТ2014. –Ґ.13. вДЦ 3. вАФ –°.
68-76. - –Ъ–∞–і—Г—А–Є–љ–∞, –Ґ. –Ш. –Ф–Є—Б–њ–ї–∞–Ј–Є—П —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є : —А—Г–Ї. –і–ї—П –≤—А–∞—З–µ–є / –Ґ. –Ш. –Ъ–∞–і—Г—А–Є–љ–∞, –Т. –Э. –У–Њ—А–±—Г–љ–Њ–≤–∞. вАФ –°–Я–±. : –≠–Ы–С–Ш- –°–Я–±, 2009. вАФ 704 —Б.









